In-Silico-Orthopedics

Für eine effizienzbasierte individuelle Therapie muss der Zusammenhang zwischen Produktfunktion und der Pathologie des Patienten geschaffen werden. Hierzu werden biomechanische und strukturmechanische objektive Analyseprozesse benötigt, um eine fundierte Personalisierung der Medizintechnik zu ermöglichen, die nachweislich den Patienten in der Therapieentwicklung fördert.
Die personalisierte Anpassung der Produktfunktionen an den Patienten erfordert eine hohe digitale Personalisierungstechnologie, welche nur durch computergestützte Verfahren möglich wird. Aufgrund der daraus resultierenden Komplexität der Produktfunktionen, der Auslegung, der Herstellung und der Digitalisierung müssen strategische Konzepte entwickelt werden, die für eine digitale Zukunft richtungsweisend sind. Zusätzlich wird die Nachhaltigkeit von Produktlebenszyklen immer wichtiger für die Akzeptanz von Produkten. In diesem Zusammenhang drängen biobasierte Materialen immer stärker in den Markt. Durch bioinspirierte Funktionsintegration in personalisierten Produkten können neue nachhaltige Lösungen geschaffen werden. Gleichzeitig jedoch gestaltet sich der Einstieg für viele Unternehmen in eine personalisierte digitale Produktentwicklungsstrategie schwierig, weil diverse Spitzentechnologien aus unterschiedlichen Fachbereichen dazu benötigt werden.
Das Fraunhofer IPA und das Leistungszentrum »Mass Personalization« stellen sich dieser Herausforderung, um bestehende Risiken und Innovationsbarrieren im Dienste des Wirtschaftsstandorts Deutschland abzubauen.
Experimentelle Biomechanik
Experimentelle Analysen des Bewegungsapparats sind für die Diagnose von orthopädischen Pathologien essentiell. Es bestehen diverse Möglichkeiten, Analysedaten des Bewegungsapparates zu erstellen, z. B. Kinetik- und Kinematikdaten aus der biomechanischen Bewegungsanalyse, medizinische Bilddaten aus MRT-, CT-, Röntgen- oder Ultraschallaufnahmen zur Analyse der Anatomie, Physiologie und Biomechanik von Geweben und Gelenken. Durch die Verknüpfung dieser hochrelevanten Daten der Diagnostik entstehen neue Chancen, pathologische Zusammenhänge zu erschließen. Dazu müssen alle Messprozesse aufeinander gut abgestimmt sein. Nur durch eine exakte Registrierung der Bild- und Messdaten sind weitere Verwendungsmöglichkeiten der Daten gegeben, z.B. in computergestützten Analyseprozessen, um fundierte biomechanische Menschsimulationen zu ermöglichen oder über die Diagnoseanwendung hinaus auch für Produktentwicklungen einzusetzen.
Computergestützte Biomechanik
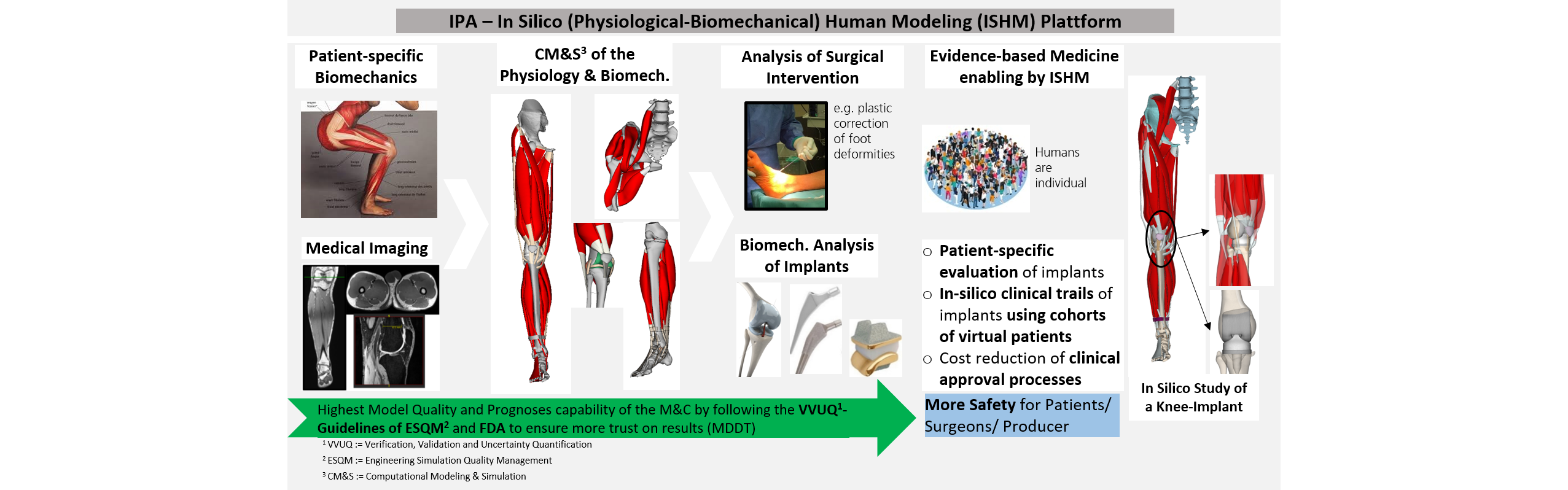
Der menschliche Bewegungsapparat ist ein komplexes System, das durch gezielte Kontraktion des Muskelsystems die Körpergliedmaßen in dynamische Bewegungen versetzt. Die Muskelkontraktionen entstehen durch physiologische (elektro-chemo-mechanische) Prozesse, die durch eine neurologische Stimulation getriggert werden. Bei vielen neuromuskulären Erkrankungen durch Parese ist das muskuläre System im Ungleichgewicht und die Steuerung der Gliedmaßen gestört. Für die realistische Analyse dieser Pathologien des muskulären Systems entwickelt das IPA eine In-silico physiological-biomechanical Human Modeling (ISHM) Plattform, womit der komplexe Bewegungsapparat mit detaillierten, prognosefähigen 3D-aufgelösten Menschmodellen (Muskeln, Sehnen, Bindegewebe, Ligamente, Haut, etc.) simuliert werden kann. Damit können die Folgen von Eingriffen in das sensible Muskelsystem z. B. durch rekonstruktive Chirurgie wie Achillessehnenverlängerung, Muskel- oder Sehnentransfer oder Kreuzbandersatz untersucht werden. Unser Ziel ist es, mit der ISHM-Plattform in den Entscheidungsprozess des Chirurgen mehr nachvollziehbare Evidenz einzubringen.
Personalisierte Medizintechnik durch In-silico Menschmodelle
Es stellt sich bei jedem medizintechnischen Produkt (Implantate oder Orthesen), das für einen Patienten aus dem Sortiment ausgewählt (standardisiert) oder individuell (personalisiert) hergestellt wurde, die Frage, wie groß dessen Effekt tatsächlich auf die Therapieentwicklung ist. Welchen Einfluss hat es auf die individuelle Biomechanik? Können physiologisch-biomechanische Veränderungen auftreten, die potenziell kritisch für den Bewegungsapparat sind? Ist das personalisierte Produkt wirklich überlegen gegenüber dem Standardprodukt? In der Orthopädie hat sich gezeigt, dass die beste Therapie diejenige ist, die mit minimaler Unterstützung auskommt und Überkorrekturen vermeidet. Genau diese Problemstellung adressieren wir mit unserer ISHM-Plattform, indem wir die biomechanische Wirksamkeit von Medizinprodukten patientenspezifisch oder für eine definierte Patientenkohorte prüfen und optimieren. Außerdem schreibt die neue Richtlinie (MDR, Medical Device Regulation) für Medizinprodukte vor, dass für jedes Produkt die medizinische Evidenz durch klinische Studien erbracht werden muss. Allerdings sind Informationen über die Wechselwirkung zwischen Patient und Produkt aus den teuren und aufwändigen klinischen Studien oft schwer zu ziehen, weil die anatomische und physiologische Variation unter den Probanden groß und die Anzahl an Probanden begrenzt ist. In-silico klinische Studien mit beliebig großen virtuellen Patientenkohorten können dabei helfen, die Zulassungsprozesse für Produkte durch belastbare, nachvollziehbare Prüfungen von Implantaten effizienter zu gestalten und zu beschleunigen.
Personalisierte Medizintechnik durch hocheffiziente Digitalisierung
Nachhaltig bionisch-inspirierte Produkte und Produktionsprozesse
Bei Implantaten wird besonders deutlich, dass dies nicht irgendwelche einfachen Ersatzteile sind, die dem Menschen wie bei einem Auto eingesetzt werden. Man hat gelernt, dass der Körper in vielfältiger und zum Teil meist drastischer Art auf nicht adäquate Materialien und deren Eigenschaften reagiert. Je näher der Ersatz an das biologische Vorbild herankommt, desto verträglicher und damit nachhaltiger ist dieser.
Aber auch bei chirurgischen Instrumenten, die alle Funktionen erfüllen müssen, die auch von Tieren als Effektoren zum Greifen, Halten, Schneiden, Stechen, Bohren etc. verwendet werden, lohnt sich der Blick in die Natur zur Entwicklung effektiverer und effizienterer Instrumente. Insekten liefern diese Effektoren auch noch in der kleinen Größe, wie es für endoskopisches Arbeiten notwendig ist.
Diesen Blick in die Natur werfen unserer Wissenschaftler in interdisziplinärer Weise, um neue und bessere Implantate und Instrumente zu entwickeln.